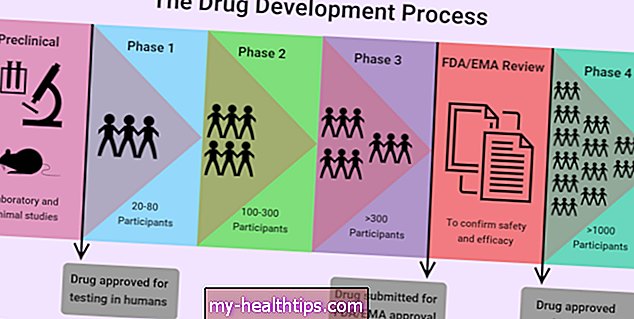
Elke fase heeft een ander doel en helpt onderzoekers verschillende vragen te beantwoorden.
- Fase I-onderzoeken. Onderzoekers testen voor het eerst een medicijn of behandeling bij een kleine groep mensen (20 tot 80). Het doel is om het medicijn of de behandeling te bestuderen om meer te weten te komen over veiligheid en om bijwerkingen te identificeren.
- Fase II-onderzoeken. Het nieuwe medicijn of de nieuwe behandeling wordt aan een grotere groep mensen (100 tot 300) gegeven om de doeltreffendheid ervan te bepalen en de veiligheid ervan verder te bestuderen.
- Fase III-onderzoeken. Het nieuwe medicijn of de nieuwe behandeling wordt aan grote groepen mensen (1.000 tot 3.000) gegeven om de doeltreffendheid ervan te bevestigen, de bijwerkingen te controleren, het te vergelijken met standaard- of vergelijkbare behandelingen en informatie te verzamelen waarmee het nieuwe medicijn of de nieuwe behandeling veilig kan worden gebruikt.
- Fase IV-onderzoeken. Nadat een medicijn is goedgekeurd door de FDA en beschikbaar is gemaakt voor het publiek, volgen onderzoekers de veiligheid ervan in de algemene bevolking, op zoek naar meer informatie over de voordelen van een medicijn of behandeling en optimaal gebruik.
Overgenomen met toestemming van NIH Clinical Trials en You. NIH onderschrijft of beveelt geen producten, diensten of informatie aan die hier door Healthline worden beschreven of aangeboden. Pagina laatst herzien op 20 oktober 2017.

.jpg)